Metais, Minerais e Minérios
Mineral designa uma substância natural presente na crosta terrestre. Interessane, também, é entender que uma rocha é um agregado de um ou mais minerais. O termo minério está associado a uma possibilidade de exploração econômica.
A bauxita é um é um mineral do qual se extraí o alumínio. E a bauxita, por sua vez, é encontrada numa rocha com uma mistura de óxido de alumínio com outras substâncias que podem ser chamadas de impureza da bauxita e após a purificação da bauxita obtêm-se a alumínia.
Um outro fator interessante se dá com a hematita, o minério de ferro. Ela pode ser apenas um mineral acessório em várias rochas (granitóides, gnaisse) porém num minério de ferro ela está muito concentrada sendo viável sua exploração econômica.
Um mineral pode ser associado a dois tipos de minerais. Um é o mineral de minério, o que possui concentrações que possibilitam a exploração econômica. E outro é chamado de ganga, este não apresenta quantidade que possibilitam uma exploração econômica. De todo modo, mineral e minério de ganga não são conceitos absolutos, porque “uma vez que um mesmo mineral pode passar de uma a outra categoria conforme o depósito mineral considerado ou até pertencer a ambas categoria em um mesmo mienério”. (TEIXEIRA, Wilson; [et al]. p. 452)
Os minerais também podem ser metálicos e não-metálicos, apesar desses termos refletirem um certo artificialismo. O mineral metálico normalmente necessita de algum trabalho para ser usado, transfomando-o em metais ou ligas metálicas, já os não-metálicos podem ser utilizados sem grandes modificações. Veja mais sobre essas categorias em: Minerais metálicos (ferrosos e não-ferrosos) e minerais não-metálicos.
Minerais metálicos (ferrosos e não-ferroso) e minerais não-metálicos.
São classificados em dois grupos: minerais metálicos e minerais não metálicos, incluindo ainda os recursos energéticos fósseis.• Minerais metálicos: que contém em sua composição elementos físicos e químicos de metal, que possibilitam uma razoável condução de calor e eletricidade. Exemplos: Ferro, alumínio e cobre.
• Minerais não metálicos: minérios que não contém em sua composição propriedades de metal. Exemplos: diamante, calcário e areia, dentre outros.
• Recursos energéticos fósseis: minérios que contém em sua composição elementos de origem orgânica. Exemplos: petróleo, gás natural e carvão.
Os minerais metálicos são encontrados em estruturas geológicas muito antigas da era pré-cambriana (proterozoica). São recursos naturais não renováveis, isto é, que não podem ser repostos pela natureza. Representam aproximadamente 4% do território brasileiro. O Brasil possui grande extensão territorial e variadas formações vegetais e geológicas; sendo assim, nosso país conta com uma grande diversidade e quantidade de recursos vegetais e minerais. No caso dos recursos minerais, temos os minerais metálicos e não-metálicos.
Os minerais metálicos servem para a produção de metais puros para uso industrial. Os metais são classificados como bens industriais porque viabilizam a expansão de várias produções fabris, de bens de produção, como equipamentos (agrícolas, industriais e de transporte), e de bens de consumo, como os materiais metálicos usados em embalagens de muitos produtos.
Metais
Os metais são substâncias muito abundantes na natureza, sendo encontrados geralmente sob a forma de minério, que é depois transformado para que se possa extrair o metal.
Em Química um metal é um elemento, substância ou liga caracterizado por sua boa condutividade elétrica e de calor, geralmente apresentando cor prateada ou amarelada, um alto ponto de fusão e de ebulição e uma elevada dureza.
Qualquer metal pode ser definido também como um elemento químico que forma aglomerados de átomos com caráter metálico. Num metal cada átomo exerce apenas uma fraca atração nos elétrons mais externos, da camada de valência, que podem então fluir livremente, proporcionando a formação de íons positivos (ou cátions) e o estabelecimento de ligações iônicas com não-metais. Os elétrons de valência são também responsáveis pela alta condutividade dos metais (teoria de bandas).
Características gerais:
- Condutibilidade: boa característica de condução térmica e elétrica;
- Maleabilidade: capacidade de ser transformado em lâminas;
- Elasticidade: capacidade de voltar ao normal após ser esticado.
Os metais apresentam grande diversidade de propriedades físicas e químicas, conforme a pressão, temperatura e outras variáveis. Diferentes tipos de mecanismos e estruturas de cristalização, o que também lhe altera as características. Geralmente, os metais apresentam ordenação cristalina simples, com alto nível de aglutinação atômica (o que implica alta densidade) e numerosos elementos de simetria. No que se refere às combinações, apresentam forte tendência a não formar compostos entre si, mas têm afinidade com elementos não metálicos como o oxigênio e o enxofre, com os quais formam, respectivamente, óxidos e sulfetos. O tamanho, forma e disposição das partículas metálicas, especificados pela metalografia, são fundamentais para o reconhecimento das propriedades físicas que determinam a plasticidade, resistência à tração, dureza e outras propriedades do material. Esses fatores podem ser alterados por tratamentos térmicos (ciclos de aquecimento resfriamento controlados) ou mecânicos (forjamento, trefilação, laminação, etc.).
Apesar do desenvolvimento cada vez maior nos campos dos polímeros e das cerâmicas, que apresentam atualmente uma diversidade tremenda de utilizações, os metais e suas ligas continuam sendo insubstituíveis em várias de suas aplicações, principalmente no que diz respeito à confecção de materiais para construção, mecânicos ou estruturais, o que pode ser explicado principalmente pela facilidade com que são moldados, podendo assumir praticamente qualquer forma imaginável, pela condutibilidade elétrica e térmica, pela resistência física e em alguns casos, pelas propriedades magnéticas.
As propriedades dos metais:
- Têm brilho metálico.
- São geralmente sólidos à temperatura ambiente (com pouca exceções, como o Mercúrio)
- São maleáveis e dúcteis.
- São bons condutores de corrente elétrica.
- São bons condutores de calor.
- Os pontos de fusão e de ebulição são geralmente elevados, mas variam bastante.
- Apresentam uma densidade elevada.
Um metal precioso é um elemento químico metálico raro, de elevado valor econômico.
Quimicamente, os metais preciosos são menos reativos do que a maioria dos elementos, são mais lustrosos, mais suaves ou dúcteis e têm um ponto de fusão mais alto do que os outros metais. Historicamente, os metais preciosos foram importantes enquanto moeda de troca, mas atualmente são considerados principalmente como investimento e mercadoria industrial. O ouro, prata, platina e paládio cada todos um código de moeda ISO 4217.
Os metais preciosos mais conhecidos são os metais usados para a cunhagem de moedas, ouro e prata. Embora ambos tenham usos industriais, são mais conhecidos pelo seu uso arte, joalharia e moedas. Outros metais preciosos incluem os metais do grupo da platina: rutênio, ródio, paládio, ósmio, irídio e platina, sendo destes a platina a mais amplamente negociada.
A procura de metais preciosos é impulsionada por seu uso prático, mas também pelo seu papel enquanto investimento e reserva de valor. Historicamente, os metais preciosos têm preços muito mais elevados do que os metais industriais comuns.
O mineral
O ouro raramente se combina com outros elementos, sendo, por isso, encontrado na natureza geralmente no estado nativo. Cristaliza na forma de cubos e octaedros, mas é muito mais
 |
| Pepita de Ouro |
comum encontrá-lo na forma de escamas, massas irregulares (pepitas) ou fios irregulares. É opaco e tem cor amarela típica, mas, quando pulverizado, pode ser vermelho, preto ou púrpura. Seu brilho é metálico, a dureza baixa (2,5 a 3,0) e a densidade muito alta (19,30).
A baixa dureza permite que ele seja facilmente riscado com um canivete ou mesmo com um pedaço de vidro. Devido à alta maleabildiade, quando martelado amassa em vez de quebrar. Se mordido, fica com marcas dos dentes. O brilho não é muito intenso, ao contrário do que muitos pensam.
A pirita, é um sulfeto de ferro que, por sua semelhança com o ouro, é chamada popularmente de ouro dos trouxas ou ouro dos tolos. Ela é, na verdade, até bem diferente do ouro. É bem mais leve que ele, não é maleável e seu brilho costuma ser bem mais forte. E, ao contrário do ouro, é comum aparecer na forma de belos cristais.
O ouro ocorre em aluviões e em veios de quartzo associados a rochas intrusivas ácidas. É encontrado também como teluretos e ligas naturais, pois geralmente contém algo de prata. Forma série isomórfica com a prata, ou seja, a mistura ouro-prata pode ocorrer em todas as proporções.
Está muito disseminado na crosta terrestre, geralmente associado ao quartzo ou à pirita. Estima-se haver quase nove milhões de toneladas de ouro dissolvido na água do mar. Um dos poucos elementos com o qual o ouro se combina é o telúrio, formando teluretos. Assim, este metal é encontrado em minerais como krennerita, calaverita e silvanita. A liga com prata chama-se eletro.
O metal
O ouro é o mais maleável e o mais dúctil dos metais. Com 1 g desse metal, podem-se obter até 2.000 m de fio ou lâminas de 0,96 m2 e apenas 0,0001 mm de espessura. É bom condutor de calor e eletricidade e não é afetado nem pelo ar, nem pela maioria dos reagentes químicos. Há quem o considere o mais belo dos elementos químicos. Seu ponto de fusão é 1.063 °C.
Fontes de obtenção
Os principais minerais fornecedores de ouro são ouro nativo, krennerita, calaverita, eletro, silvanita e pirita. Ele é obtido também na metalurgia de vários metais.
Estudos indicam que o metabolismo da bactéria Ralstonia metallidurans leva à formação de pepitas de ouro.
Usos
O ouro é usado principalmente em moedas; em segundo lugar, em jóias e decoração. É útil
 |
| Acervo do Metropolitan Museum of Arts (N. Iorque).Foto: P.M.Branco |
também em Odontologia (hoje muito pouco usado), instrumentos científicos, fotografia e indústria eletrônica. Para confecção de jóias, usam-se ligas com 75% de ouro (o chamado ouro dezoito quilates) ou, às vezes, com apenas 58,33% (ouro quatorze quilates). É empregado também em fotografia, na forma de ácido cloro-áurico (HAuCl4), indústria química, ligas com cobre, prata, níquel e outros metais.
A foto ao lado, mostra sandálias e dedeiras de ouro da antiga civilização egípcia. As sandálias foram escurecidas para se assemelharem ao couro.
Quem tem uma jóia e não sabe ao certo se ela é feita com ouro, deve fazer o teste usando água-régia, uma mistura de ácido nítrico com um volume três ou quatro vezes maior de ácido clorídrico, ambos concentrados. As agências de penhores da Caixa Econômica Federal fazem esse teste, que indica se a jóia é feita com ouro e se se trata de ouro 18 quilates, ou outra tipo de liga (ouro puro não se usa em jóias).
Principais produtores
É produzido principalmente na África do Sul (11 % da produção mundial em 2006), seguindo-se EUA, Austrália, China e Peru.
Entre 1700 e 1850, o Brasil foi o maior produtor de ouro no mundo, com um total de 16 toneladas no período de 1750-1754, originada predominantemente das aluviões da região do Quadrilátero Ferrífero, em Minas Gerais. A importância do Brasil continuou crescente até à primeira metade do século XIX, quando perdeu a liderança diante das grandes descobertas de ouro aluvionar da Califórnia, nos Estados Unidos.
Entre 1965 e 1996, nossa produção alcançou 877 toneladas, representando cerca de 4% da produção mundial.
O ouro brasileiro é extraído principalmente em Minas Gerais e no Pará. Em 2003, a produção foi de 40,4 t e em 2004, de 47,6 t de ouro.
Segundo o Mapa de Reservas de Ouro do Brasil, elaborado em 1998 pelo Serviço Geológico do Brasil, as reservas em ouro brasileiras são estimadas em 2.283 toneladas.
Preço
O preço do ouro varia constantemente, já que é muito usado como investimento. Em 29 de junho de 2007, a onça-troy (31,103 gramas) valia US$ 647, metade do preço da platina (US$ 1.273), mas quase o dobro do preço do paládio (US$ 365).
Curiosidades
Estima-se que todo o ouro do planeta daria para fazer um cubo de 15 m de aresta. Em 1999, joalheiros de Dubai fizeram a maior corrente de ouro do mundo: 4.382 m. Usaram ouro 22 quilates e gastaram cerca de US$ 2 milhões. A peça foi vendida em praça pública, em pedaços.
A Prata
O elemento químico
A prata é o elemento de número atômico 47 e massa atômica 107,87. É um metal do grupo 1B, como o ouro e o cobre.
O mineral
A prata cristaliza no sistema cúbico (como o ouro), e seus cristais podem ser cubos, dodecaedros ou octaedros. Entretanto, eles são raros, e o mineral é geralmente acicular, fibroso, dendrítico ou irregular.
 |
| Prata de habito filiforme Fonte: Korbel,P. & Novák,M. Enciclopédia de Minerais |
Tem cor cinza (prateada) , inclusive quando em pó. Não tem clivagem. Sua dureza é baixa (2,5 a 3,0) e a densidade, alta (10,50), mas muito inferior à do ouro. Ocorre em filões. Possui intenso brilho metálico, que enfraquece se o ar contiver enxofre, o que geralmente ocorre nas cidades.
O metal
A prata é um metal muito dúctil e maleável. Permite obter lâminas com 0,003 mm de espessura e fios de 100 m pesando apenas 38 mg. Duas peças de prata podem ser soldadas a marteladas, desde que aquecidas a 600ºC. Seu ponto de fusão é 960 °C. É o metal que melhor conduz o calor e a eletricidade. Tem propriedades semelhantes às do Cu e do Au.
Fontes de obtenção
A prata forma 129 minerais, sendo extraída de muitos deles, como pirargirita, argentita, acantita, cerargirita, galena argentífera, stromeyerita, tetraedrita, pearceíta, proustita, stephanita, tennantita, polibasita, silvanita e prata nativa. Pode ser obtida também como subproduto na metalurgia do zinco, do ouro, do níquel e do cobre. Ela está muitíssimo menos disseminada que o ouro na natureza.
Usos
Usa-se prata na joalheria, em moedas, espelhos, talheres, na Odontologia (como amálgama), soldas, explosivos (fulminato), chuvas artificiais (iodeto), óptica (cloreto), fotografia (nitrato), germicida, objetos ornamentais e em ligas com cobre. Para jóias e objetos ornamentais, usam-se ligas com 10% cobre (prata 90 ou prata 900) ou, mais freqüentemente, 95% de prata (prata 950).
Principais produtores
O maior produtor de prata é o México, com 2.748 t (dados de 2002), seguindo-se Peru, China e Austrália, todos com mais de 2.000 t. O Brasil produziu, em 2002, apenas 10 t, em Minas Gerais e, sobretudo, no Paraná, como subproduto do chumbo. Curiosidade A maior pepita de prata conhecida foi encontrada em Sonora (México) e tinha 1.026 kg.
Prata de Lei
No século XIII, o rei de Portugal Dom Afonso II promulgou uma lei que punia severamente quem alterasse o teor da mistura da prata.
Era em conformidade com essa lei a liga de prata que contivesse, no mínimo, 80% de prata pura em sua composição.
Esse termo, prata de lei, é usado, ainda hoje, para denominar os diversos tipos de ligas de prata, especialmente as chamadas “pratas baixas”, as ligas com teor inferior a 925 gramas de prata por mil gramas.
Além do banho de prata, esses objetos recebem uma camada de verniz especial que impede a oxidação durante cerca de 12 meses, dependendo dos cuidados. Esses objetos, se usados no dia-a-dia, podem perder o brilho rapidamente .
Um metal precioso
A prata é, juntamente com o ouro, um metal precioso usado por homens e mulheres desde a antigüidade.
Algumas pessoas desinformadas consideram as jóias em prata como semijóias ou bijuterias, o que é um grande erro.
Essa denominação de “semijóia” somente é adequada quando se trata de peças banhadas em prata e não peças maciças. (Na verdade, falar em “semijóia” é tão fora de propósito como falar em ovos semi-estragados, mulher semigrávida ou pedras semipreciosas.)
A prata possui variadas gradações que indicam o seu nível de pureza.
A prata pura ou prata fina possui o teor de pureza igual a 1000 e não se usa na fabricação de jóias, a não ser em casos especiais como filigrana.
Peças confecciondas com prata 1000 ficam com um grau de dureza muito baixo e se arranham ou se machucam facilmente.
As ligas mais usadas
• Prata 950 – contém 5% de liga. É a ideal para a fabricação de jóias artesanais. Apresenta alto brilho e ótimo grau de dureza.
• Prata 925 – Contém 7,5% de liga de cobre.
• Prata 90 ou 900 – é a de menor valor.
Depois de fundida, em altas temperaturas, é usada para banhar objetos de latão, de cobre, de ferro e de estanho, entre outros metais.
PRATA DE LEI (925 ou 950):
É a prata utilizada na fabricação de jóias. Ela é pura e tem como liga, no máximo, 7,5% de outros metais. A cada 1000 partes de metal, 950 são de prata. As outras 50 pertencem a outros metais, normalmente Cobre.
Prata Leve
É uma composição de metais leves, aditivada com prata, camada isolante de ouro 18K e acabamento final com prata pura. As jóias desta linha possuem leveza e brilho únicos.
Oxidação – Toda oxidação é superficial e deve-se : a reação do organismo, “stress”, suor ou contato com cosméticos, perfumes, gazes etc.
Ácido úrico – Pessoas que possuem o ácido úrico muito elevado devido a algum problema de saúde também escurecem a peça.
A Platina
O elemento químico
A platina é o elemento químico de número atômico 78 e massa atômica 195,09. Pertence ao grupo 8B das tabela periódica, junto com o níquel e o paládio.
O mineral
A platina é um mineral do sistema cúbico, geralmente encontrada em grãos irregulares, raramente em octaedros ou cubos. Tem cor cinza-aço, traço cinza brilhante, brilho metálico, sem clivagem. É, às vezes, magnética. Tem dureza 4,0 a 4,5 e densidade 21,40 (altíssima).
 |
| Cristal de platina(Fonte: Korbel,P. & Novák,M. Enciclopédia de MineraisO mineral |
O metal
A platina é um metal maleável, dúctil, resistente à corrosão pelo ar, solúvel em água-régia. Absorve hidrogênio como o paládio. Provoca explosão do hidrogênio ou do oxigênio. Seu ponto de fusão é 1.773,5 °C.
Fontes de obtenção
Pode ser extraída de vários minerais: sperrylita, platinirídio, polixênio, cooperita e ferroplatina. A platina nativa ocorre na natureza geralmente misturada com ferro, irídio, paládio e níquel. Ocorre em rochas básicas, como dunitos, piroxenitos e gabros, e em aluviões.
Usos
É empregada em joalheria (com 35% de paládio e 5% de outros metais), instrumental para laboratório, Odontologia, eletricidade, ogivas de mísseis, catalisadores, pirômetros, liga com cobalto, fornos elétricos de alta temperatura, fotografia e em vários outros produtos industriais.
Principais produtores
A platina é produzida principalmente pela África do Sul (134 t em 2002), seguindo-se Rússia (35 t), Canadá (7 t) e EUA (4,39 t).
Preço
Em 29 de junho de 2007, a onça-troy de platina valia US$ 1.273, quase o dobro do preço do ouro (US$ 647).
Curiosidades
Em 1985, foi exposto em Tóquio (Japão) um vestido feito a mão, com fios de platina, pesando 12 kg e avaliado em um milhão de dólares.
O Paládio
O elemento químico
O paládio tem número atômico 46 e massa atômica 106,4. Pertence ao mesmo da platina (8B).
O mineral
É um mineral do sistema cúbico, de cor cinza-aço, que ocorre na forma de grãos (pepitas), às vezes com estrutura fibrorradiada. É séctil, de brilho metálico. Tem dureza. 4,5 a 5,0 e densidade 11,40.
O metal
O pládio é inoxidável, dúctil e muito maleável, podendo ser reduzido a folhas de 0,0001 mm de espessura. Seu ponto de fusão é 1.500 °C. Tem notável capacidade de absorção de hidrogênio (até 900 vezes seu próprio volume), formando, possivelmente, PdH2.
Fontes de obtenção
O paládio é extraído dos minerais de platina.
Usos
É usado como catalisador, em instrumentos odontológicos (Prótese e Ortodontia) e cirúrgicos, relojoaria e joalheria (neste caso, como substituto da platina). Forma ligas com ouro (ouro marrom, ouro branco-médio, ouro branco-suave).
Principais produtores
Em 2002, o maior produtor de paládio foi a Rússia (84 t), seguindo-se África do Sul, Estados Unidos e Canadá.
Preço
Em 29 de junho de 2007, a onça-troy de paládio valia US$ 365, pouco mais da metade do valor do ouro (US$ 647).
Curiosidades
O nome do paládio deriva de Pallas, planetóide descoberto em 1802, um ano antes de se descobrir o elemento. O mineral paládio foi descoberto pela primeira vez em Morro do Pilar, MG (Brasil).
Tipos de Metal
Existem muitos tipos de metais, chegando hoje ao total de sessenta e oito. Dentre eles existem alguns bem diferentes, como o mercúrio (que é líquido) e o sódio (que é leve). Os mais conhecidos e utilizados há muitos anos são o ferro, cobre, estanho, chumbo, ouro e a prata.
Os metais podem ser separados em dois grandes grupos: os ferrosos (compostos por ferro) e os não-ferrosos.
Veja abaixo os principais tipos de metais e suas aplicações:
|
Tipos |
Aplicações |
|
| FERROSOS | ||
| Ferro | utensílios domésticos, ferramentas, peças de automóveis estruturas de edifícios, latas de alimentos e bebidas; | |
| Aço | latas de alimentos, peças de automóveis, aço para a construção civil; | |
| NÃO-FERROSOS | ||
| Alumínio | latas de bebidas, esquadrias; | |
| Cobre | cabos telefônicos e enrolamentos elétricos, encanamentos; | |
| Metais pesados | Chumbo | baterias de carros, lacres; |
| Níquel | baterias de celular; | |
| Zinco | telhados, baterias | |
| Mercúrio | lâmpadas fluorescentes, baterias | |
ALUMÍNIO
Sua História
A história do alumínio e de suas múltiplas aplicações no mundo moderno é remota. Apesar de ser o mais abundante metal do planeta, ele não se encontra naturalmente na forma metálica e foi somente em 1824 que o dinamarquês Hans Christian Oersted conseguiu isolar o alumínio na forma como é hoje conhecido. Atualmente possui inúmeras aplicações como na fabricação de panelas, janelas, peças de carro, equipamentos eletrônicos, latas de bebidas etc.
Composição
O alumínio é obtido a partir do minério bauxita. Vale ressaltar que o processo de extração deste minério, assim como dos demais, é atividade que provoca intenso impacto do solo e dos corpos hídricos. Para extrair o alumínio é feito um processo de refino da bauxita que resulta em um pó branco, parecido com o açúcar, a alumina. Em seguida a alumina passa por um processo eletroquímico e é transformada em alumínio.
Reciclagem de alumínio
Este metal é 100% reciclável, em número ilimitado de vezes e quando se recicla o alumínio, são economizados 95% da energia que foi necessária para produzí-lo da primeira vez.
Boa parte do alumínio destinado à reciclagem é proveniente das embalagens, em especial latas de bebidas.
As latinhas recuperadas são transformadas em lingotes que posteriormente são empregados na fabricação de novas latas e inúmeros outros produtos de alumínio.
Atualmente o Brasil é o país que mais recicla latas alumínio no mundo, porém, vale destacar que isso é consequência da falta de oportunidade no mercado de trabalho, se apresentando como alternativa de subsistência para grande parte da população. Mesmo aumentando o material destinado à reciclagem, não houve redução na extração do minério bauxita, atividade esta de intenso impacto ambiental como já mencionado acima.
Índice de reciclagem de latas de alumínio no Brasil
|
2001 |
85% |
|
2002 |
87% |
|
2003 |
89% |
|
2004 |
96% |
Reciclagem da lata de alumínio
Fonte: Abralatas
Para saber mais sobre o assunto entre em contato com:
LATASA
www.latasa.com.br
tel.: (21)2589-8867
ABRALATAS – Associação Brasileira dos Fabricantes de Latas de Alta Reciclabilidade
(61)327-2142
ABAL – Associação Brasileira do Alumínio
(11) 5084-1544
FONTES:
Abralatas
ABAL
IPT-CEMPRE, 2000
AÇO
Sua História
O ferro foi descoberto ainda na pré-história, porém, o aço, como conhecemos atualmente, só foi desenvolvido em 1856, alcançando grande repercussão no meio industrial. Isso porque o aço é mais resistente que o ferro fundido e pode ser produzido em grandes quantidades, servindo de matéria-prima para muitas indústrias.
Com o avanço tecnológico dos fornos e a crescente demanda por produtos feitos de ferro e aço, as indústrias siderúrgicas aumentaram a produção. No entanto, o crescimento deste setor trouxe também um aumento da extração de madeira para produção de carvão e da emissão de gases poluentes na atmosfera pela queima de carvão vegetal.A produção mundial de aço bruto, em 2003, foi de cerca de 965 milhões de toneladas anuais. Para 2004, a expectativa é de que ela ultrapassará um bilhão de toneladas.
O ferro e o aço são encontrados na agricultura (ceifadeiras, colheitadeiras, semeadores, arados, etc.), nos transportes (caminhões, carros, navios, aviões etc.), na construção civil, na indústria automobilística, em embalagens, aparelhos domésticos e muitas outras utilidades.
As latas de aço e flandres são amplamente utilizadas no mercado nacional de embalagens principalmente para o armazenamento de alimentos, óleos lubrificantes, tampas metálicas e outros.
Composição
Para a obtenção das chapas de aço é necessário extrair da natureza o minério de ferro, denominado hematita, e a partir de sua redução com carvão vegetal, produz-se uma chapa com alto grau de pureza.
As latas de aço produzidas com chapas metálicas, conhecidas como folhas de flandres, são compostas por ferro e uma pequena parte de estanho (0,20%) ou cromo (0,007%), materiais que as protegem contra a oxidação (ferrugem).
Reciclagem de aço
A reciclagem de aço remonta à própria história de utilização do metal. Reciclado, mantém suas propriedades como dureza, resistência e versatilidade. As latas normalmente jogadas no lixo podem retornar a nós em forma de novas latas, ou como vários utensílios – arames, partes de automóvel, dobradiças, maçanetas e muitos outros.
Nas áreas de armazenamento, as latas são prensadas para aumentar sua densidade e melhorar as condições de transporte. São enviadas às indústrias siderúrgicas junto com as demais sucatas metálicas, para se transformarem em tarugos ou folhas de flandres.
As latas de aço lançadas na natureza sofrem oxidação num prazo médio de 3 anos, transformando-se em óxidos ou hidróxidos de ferro. Se recuperadas, podem ser recicladas infinitamente.
Índice de reciclagem de latas de aço no Brasil
|
2003 |
47% |
Se considerarmos os índices de reciclagem de carros velhos, eletrodomésticos, resíduos de construção civil, ou seja, todos os segmentos do aço, e somarmos aos índices das embalagens de aço, o Brasil recicla cerca de 70% de todo o aço produzido anualmente.
Para saber mais sobre o assunto entre em contato com:
ABEAÇO – Associação Brasileira de Embalagem de Aço
0800172044 (Disk aço)
CEMPRE – Compromisso Empresarial para Reciclagem
(11) 3889-7806
IBS – Instituto Brasileiro de Siderurgia
(21) 2141-0001
Sindivesfa/INESFA
(11) 251-0277
FONTES:
IBS
ABEAÇO
IPT-CEMPRE, 2000
Calderoni, 1997
UM CASO ESPECIAL: OS METAIS PESADOS
A maioria dos organismos vivos só precisa de alguns poucos metais e em doses muito pequenas, por isso são chamados de micronutrientes. Este é o caso do zinco, do magnésio, do cobalto e do ferro. Estes metais tornam-se tóxicos e perigosos para a saúde humana quando ultrapassam determinadas concentrações-limite.
Já o chumbo, o mercúrio, o cádmio, o cromo e o arsênio são metais que não existem naturalmente em nenhum organismo. Tampouco desempenham funções – nutricionais ou bioquímicas – em microorganismos, plantas ou animais. Ou seja: a presença destes metais em organismos vivos é prejudicial em qualquer concentração. Desde que o homem descobriu a metalurgia, a produção destes metais aumentou e seus efeitos tóxicos geraram problemas de saúde permanentes, tanto para seres humanos como para o ecossistema.
|
DEFINIÇÃO: Grupo dos metais de alto peso molecular, de particular efeito danoso aos seres vivos por não serem biodegradáveis e se acumularem no organismo e em diversas cadeias alimentares, incluindo as cadeias dos quais os homens fazem parte, podendo provocar sérias doenças como câncer, por exemplo. Este termo tem sido também aplicado a elementos que, embora possuam estas características, não são rigorosamente metais. |
Normalmente, os metais pesados apresentam-se em concentrações muito pequenas, associados a outros elementos químicos, formando minerais em rochas. Quando lançados na água como resíduos industriais, podem ser absorvidos pelos tecidos animais e vegetais.
Estas substâncias tóxicas também depositam-se no solo ou em corpos d’água de regiões mais distantes, graças à movimentação das massas de ar. Assim, os metais pesados podem se acumular em todos os organismos que constituem a cadeia alimentar do homem. É claro que populações residentes em locais próximos a indústrias ou incineradores correm maiores riscos de contaminação.
Outra fonte importante de contaminação do ambiente por metais pesados são os incineradores de lixo urbano e industrial, que provocam a sua volatilização e formam cinzas ricas em metais, principalmente mercúrio, chumbo e cádmio.
Principais metais pesados e seus Impactos:
|
Metal |
Fontes Principais | Impactos na saúde e no meio ambiente |
|
Chumbo |
|
|
|
Cádmio |
|
|
|
Mercúrio |
|
|
|
Alumínio |
Produção de artefatos de alumínio; serralheria; soldagem de medicamentos (antiácidos) e tratamento convencional de água. | Anemia por deficiência de ferro; intoxicação crônica |
|
Arsênio |
Metalurgia; manufatura de vidros e fundição | Câncer (seios paranasais) |
|
Cobalto |
Preparo de ferramentas de corte e furadoras | Fibrose pulmonar (endurecimento do pulmão) que pode levar à morte |
|
Cromo |
Indústrias de corantes, esmaltes, tintas, ligas com aço e níquel; cromagem de metais | Asma (bronquite); câncer |
|
Fósforo amarelo |
Veneno para baratas; rodenticidas (tipo de inseticida usado na lavoura) e fogos de artifício. | Náuseas; gastrite; odor de alho; fezes e vômitos fosforescentes; dor muscular; torpor; choque; coma e até morte |
|
Chumbo |
Fabricação e reciclagem de baterias de autos; indústria de tintas; pintura em cerâmica; soldagem | Saturnismo (cólicas abdominais, tremores, fraqueza muscular, lesão renal e cerebral) |
|
Níquel |
Baterias; aramados; fundição e niquelagem de metais; refinarias | Câncer de pulmão e seios paranasais |
|
Fumos metálicos |
Vapores (de cobre, cádmio, ferro, manganês, níquel e zinco) da soldagem industrial ou da galvanização de metais. | Febre dos fumos metálicos (febre, tosse, cansaço e dores musculares) – parecido com pneumonia. |
¹ Crianças são especialmente vulneráveis aos efeitos do chumbo. Mesmo quantidades relativamente pequenas de chumbo podem causar rebaixamento permanente da inteligência em crianças, potencialmente resultando em desordens para leitura, distúrbios psicológicos e retardamento mental. Outros efeitos em crianças incluem doenças nos rins e artrite.
Reciclagem de materiais pesados
1. Pilhas:
A reciclagem de pilhas envolve geralmente três fases: a triagem, o tratamento físico e o tratamento metalúrgico. O tratamento físico consiste na moagem e posterior separação de constituintes. O tratamento metalúrgico depende da tecnologia adotada pela unidade de reciclagem, podendo ser:
Processo Pirometalúrgico – após a moagem, o ferro é separado magneticamente. Os outros metais são separados tendo em conta os diferentes pontos de fusão. Uma queima inicial permite a total recuperação do mercúrio e do zinco nos gases de saída. O resíduo é então aquecido acima de 1000ºC com um agente redutor, ocorrendo nesta fase a reciclagem do magnésio e de mais algum zinco. Trata-se, portanto, de um processo térmico que consiste em evaporar à temperatura precisa cada metal para recuperá-lo depois, por condensação.
Processo Hidrometalúrgico – opera geralmente a temperaturas que não excedem os 100ºC. As pilhas usadas, sujeitas a moagem prévia, são lixiviadas com ácido hidroclorídrico ou sulfúrico, seguindo-se a purificação das soluções através de operações de precipitação ou eletrólise para recuperação do zinco e do dióxido de magnésio, ou do cádmio e do níquel. Muitas vezes o mercúrio é removido previamente por aquecimento.
Reciclagem por tipo de pilha:
| Recarregadores de níquel-cádmio: |
- relativamente fáceis de reciclar, tanto por processos térmicos como hidrometalúrgicos;
- recuperação do cádmio é de cerca de 100% para reutilização na indústria de pilhas ou fabrico de outros produtos;
- o níquel é, geralmente, recuperado como ferro-níquel com aplicação na indústria do aço;
Pilhas primárias de “botão”:
- as pilhas primárias de botão com ânodo de zinco podem ser recicladas tanto em conjunto como separadamente para recuperação do mercúrio e da prata;
- para a mistura destes dois tipos de pilhas, os métodos geralmente em uso baseiam-se na destilação do mercúrio (processo térmico), sendo a obtenção da prata realizada à custa de um processo hidrometalúrgico, a partir dos resíduos da primeira operação;
- o tratamento de pilhas de óxido de prata (ou dos resíduos da destilação do Hg) pode também ser efetuado térmicamente, com sucata de chumbo, sendo a prata refinada por eletrólise na última etapa do processo;
- em diferentes partidas, podem ser tratados na mesma instalação outros materiais contendo mercúrio, nomeadamente as lâmpadas fluorescentes, os termômetros e amálgamas de dentistas.
Pilhas primárias cilíndricas:
- a reciclagem de pilhas primárias de zinco/dióxido de manganésio tem sido difícil de implementar pelos elevados custos associados aos processos e pelos problemas de comercialização de alguns dos produtos obtidos na operação.
2. Descontaminação de metais pesados no solo:
Foram os cientistas da Universidade Ehime (Japão) os descobridores desta nova tecnologia de limpeza de solos contaminados por metais pesados que poderá ser a solução para a recuperação de aterros sanitários ou de regiões atingidas por acidentes com produtos químicos. O que é mais interessante no novo processo é que os metais pesados são separados e podem ser reutilizados em processos industriais, eliminando a necessidade da criação de novos locais de deposição de resíduos. O método também pode ser utilizado para limpeza de águas contaminadas.
O novo método faz com que os metais pesados no solo precipitem-se com elementos de ferro contidos no próprio solo, sendo então recuperados e separados. A tecnologia permite a seleção de quais metais pesados devem ser retirados, permitindo um controle ativo sobre o processo de limpeza do solo. O equipamento envolvido é de pequeno porte, podendo ser levado ao local da descontaminação, evitando a remoção de solo contaminado, o que sempre abre possibilidades para novos acidentes.
A nova tecnologia remove os metais pesados de maneira seletiva e os recupera no próprio local da contaminação, redepositando o solo já descontaminado no lugar, evitando a necessidade de relocalização e a retirada de solo de outro local.
…
Mineral é um corpo natural sólido e cristalino formado em resultado da interacção de processos físico-químicos em ambientes geológicos. Cada mineral é classificado e denominado não apenas com base na sua composição química, mas também na estrutura cristalina dos materiais que o compõem. Em resultado dessa distinção, materiais com a mesma composição química podem constituir minerais totalmente distintos em resultado de meras diferenças estruturais na forma como os seus átomos ou moléculas se arranjam espacialmente (como por exemplo a grafite e o diamante). Os minerais variam na sua composição desde elementos químicos, em estado puro ou quase puro, e sais simples a silicatos complexos com milhares de formas conhecidas. Embora em sentido estrito opetróleo, o gás natural e outros compostos orgânicos formados em ambientes geológicos sejam minerais, geralmente a maioria dos compostos orgânicos é excluída. Também são excluídas as substâncias, mesmo que idênticas em composição e estrutura a algum mineral, produzidas pela actividade humana (como por exemplos os betões ou os diamantes artificiais). O estudo dos minerais constitui o objecto da mineralogia.
Estrutura cristalina

Estrutura cristalina de um cristal de sal (NaCl). Note-se a ordenação dos átomos.
Um dos pilares fundamentais do estudo dos minerais, e um dos elementos determinantes na sua classificação, é a determinação da sua estrutura cristalina (ou ausência dela), já que esse factor determina, a par com a composição química, a generalidade das propriedades do material e fornece indicações claras sobre os processos e ambientes geológicos que estiveram na sua origem, bem como o tipo de rochas de que poderá fazer parte.
Neste contexto, estrutura cristalina significa o arranjo espacial de longo alcance em que se encontram os átomos ou moléculas no mineral. Na natureza existem 14 arranjos básicos tridimensionais de partículas (neste caso átomos ou moléculas, entenda-se), designados por redes de Bravais, agrupados em 7 sistemas de cristalização distintos, que permitem descrever todos os cristais até agora encontrados (as excepções conhecidas são os quase cristais de Shechtman, os quais, contudo, não são verdadeiros cristais por não possuírem uma malha com repetição espacial uniforme).
É portanto da conjugação da composição química e da estrutura cristalina que é definido um mineral, sendo em extremo comuns substâncias que em condições geológicas distintas cristalizam em formas diferentes, para não falar da similaridade de cristalização por parte de substâncias com composição química totalmente diversa.
De facto, dois ou mais minerais podem ter a mesma composição química, mas estruturas cristalinas diferentes, sendo nesse caso conhecidos como polimorfos do mesmo composto. Por exemplo, a pirite e a marcassite são ambos constituídos por sulfeto de ferro, embora sejam totalmente distintos em aspecto físico e propriedades.
Similarmente, alguns minerais têm composições químicas diferentes, mas a mesma estrutura cristalina, originando isomorfos. Um exemplo é dado pela halite, um composto de sódio e cloro em tudo similar ao vulgar sal de cozinha, a galena, um sulfeto de chumbo, e a periclase, um composto de magnésio e oxigénio. Apesar de composições químicas radicalmente diferentes, todos estes minerais compartilham da mesma estrutura cristalina cúbica.
As estruturas cristalinas determinam de forma preponderante as propriedades físicas de um mineral: apesar do diamante e grafite terem a mesma composição, a grafite é tão branda que é utilizada como lubrificante, enquanto o diamante é o mais duro dos minerais, o qual é derivado do carbono.
Para ser classificado como um “verdadeiro” mineral, uma substância deve ser um sólido e ter uma estrutura cristalina definida. Deve também ser uma substância homogénea natural com uma composição química definida. Substâncias semelhantes a minerais que não satisfazem estritamente a definição, são por vezes classificados como mineralóides.
Estão actualmente catalogados mais de 4 000 minerais, todos eles reconhecidos e classificados de acordo com a International Mineralogical Association (IMA), a instituição de referência na aprovação da classificação e nomenclatura internacional dos minerais.
De fora ficam materiais como a obsidiana ou o âmbar, que embora tenham carácter homogéneo, origem geológica e aspecto mineral dado pela sua origem, ocorrência e características macroscópicas, não são materiais cristalinos.
Minerais e rochas
Embora na linguagem comum por vezes os termos mineral e rocha sejam utilizados de forma quase sinónima, é importante manter uma distinção clara entre ambos. É preciso não perder de vista que um mineral é um composto químico com uma determinada composição química e uma estrutura cristalina definida, como atrás foi apontado. Se é verdade que existem rochas compostas por um único mineral, na generalidade dos casos, uma rocha é uma mistura complexa de um ou diversos minerais, em proporções variadas, incluindo frequentemente fracções, que podem ser significativas ou mesmo dominantes, de material vítreo, isto é, não cristalino.
Os minerais específicos numa rocha, ou seja aqueles que determinam a classificação desta, variam muito. Alguns minerais, como o quartzo, a mica ou o talco apresentam uma vasta distribuição geográfica e petrológica, enquanto outros ocorrem de forma muito restrita. Mais de metade dos mais de 4000 minerais reconhecidos são tão raros que foram encontrados somente num punhado das amostras, e muitos são conhecidos somente por alguns pequenos cristais. Pondere-se a diferença de abundância entre o quartzo e odiamante, sendo certo que este último é um dos minerais mais raros.
Propriedades físicas dos minerais
As propriedades físicas dos minerais resultam da sua composição química e das suas características estruturais. As propriedades físicas mais óbvias e mais facilmente comparáveis são as mais utilizadas na identificação de um mineral. Na maioria das vezes, essas propriedades, e a utilização de tabelas adequadas, são suficientes para uma correcta identificação. Quando tal não é possível, ou quando um elevado grau de ambiguidade persiste, como no caso de muitos isomorfos similares, a identificação é realizada a partir da análise química, de estudos de óptica ao microscópio petrográfico ou por difracção de raios X ou de neutrões. São as seguintes as propriedades físicas macroscópicas, isto é observáveis sem necessidade de equipamento sofisticado (por vezes designadas, por essa razão, por propriedades de campo).
Cor
É uma característica extremamente importante dos minerais. Pode variar devido a impurezas existentes em minerais como o quartzo, o corindo, a fluorite, a calcite e a turmalina, entre outros. Em outros casos, a superfície do mineral pode estar alterada, não mostrando sua verdadeira cor. A origem da cor nos minerais está principalmente ligada à presença de iões metálicos, fenómenos de transferência de carga e efeitos da radiação ionizante. Eis alguns exemplos:
- Jadeíte — esverdeado;
- Augita — verde escuro a preto;
- Cassiterita — verde a castanho;
- Pirita — amarelo-ouro
Brilho
O brilho depende da absorção, refracção ou reflexão da luz pelas superfícies frescas de fractura do mineral (ou as faces dos seus cristais ou as superfícies de clivagem). O brilho é avaliado à vista desarmada e descrito em termos comparativos utilizando um conjunto de termos padronizados. Os brilhos são em geral agrupados em: metálico e não metálico ouvulgar. Diz-se que o brilho é não metálico, ou vulgar, quando não é semelhante aos dos metais, sendo característico dos minerais transparentes ou translúcidos. Dentro das grandes classes atrás apontadas, o brilho de um mineral pode ser descrito como:
- Brilhos não metálicos:
- Acetinado — brilho não metálico que faz lembrar o brilho do cetim; é característico dos minerais fibrosos;
- Adamantino — brilho não metálico que, pelas suas características, nomeadamente a intensidade, se assemelha ao do diamante (são exemplos a pirargirita e a cerussita;
- Ceroso — brilho não metálico que lembra o da cera (é exemplo a variscita);
- Nacarado — brilho não metálico semelhante ao das pérolas (é exemplo a caulinita);
- Resinoso — brilho não metálico que lembra o observado nas superfícies de fractura das resinas (é exemplo a monazita);
- Vítreo — brilho não metálico que lembra o do vidro (são exemplos a fluorita, a halita e a aragonita);
- Brilhos metálicos:
- Metálico — brilho que se assemelha ao dos metais, sendo característico de minerais opacos como a galena, a calcopirita e a pirita;
- Submetálico — brilho que faz lembrar o dos metais, mas não tão intenso, sendo característico dos minerais quase opacos como a cromita.
Traço (ou risca)
A cor do traço de um mineral pode ser observada quando uma louça ou porcelana branca é riscada. A clorite, a gipsita (gesso) e o talco deixam um traço branco, enquanto ozircão, a granada e a estaurolita deixam, comummente, um traço castanho avermelhado. O traço de um mineral fornece uma importante característica para sua identificação, já que permite diferenciar materiais com cores e brilhos similares.
Clivagem
É a forma como muitos minerais se quebram seguindo planos relacionados com a estrutura molecular interna, paralelos às possíveis faces do cristal que formariam. A clivagem é descrita em cinco modalidades: desde pobre, como na bornita; moderada; boa; perfeita; e proeminente, como nas micas. Os tipos de clivagem são descritos pelo número e direcção dos planos de clivagem.
Fractura
Refere-se à maneira pela qual um mineral se parte, excepto quando ela é controlada pelas propriedades de clivagem e partição. O estilo de fracturação é um elemento importante na identificação do mineral. Alguns minerais apresentam estilos de fracturação muito característicos, determinantes na sua identificação. Minerais com fractura conchoidal, por exemplo, são: quartzo, zircão, ilmenita, calcedônia, opala, apatita.
Dureza
Expressa a resistência de um mineral à abrasão ou ao risco. Ela reflete a força de ligação dos átomos, iões ou moléculas que formam a estrutura. A escala de dureza mais frequentemente utilizada, apesar da variação da dureza nela não ser gradativa ou proporcional, é a escala de Mohs, que consta dos seguintes minerais de referência (ordenados por dureza crescente):
- 1 – Talco;
- 2 – Gesso;
- 3 – Calcita;
- 4 – Fluorita;
- 5 – Apatita;
- 6 – Ortoclásio;
- 7 – Quartzo;
- 8 – Topázio;
- 9 – Corindon;
- 10– Diamante.
Densidade
É a medição directa da densidade mássica, medida pela relação directa entre a massa e o volume do mineral.
Tenacidade
Mede a coesão de um mineral, ou seja, a resistência a ser quebrado, dobrado ou esmagado. A tenacidade não reflecte necessariamente a dureza, antes sendo dela geralmente independente: o diamante, por exemplo, possui dureza muito elevada (é o termo mais alto da escala de Mohs), mas tenacidade relativamente baixa, já que quebra facilmente se submetido a um impacto. A tenacidade dos minerais é expressa em termos qualitativos, utilizando uma linguagem padronizada:
- Quebradiço ou frágil – o mineral parte-se ou é pulverizado com facilidade;
- Maleável – o mineral, por impacto, pode ser transformado em lâminas;
- Séctil – o mineral pode ser cortado por uma lâmina de aço;
- Dúctil – o mineral pode ser estirado para formar fios;
- Flexível – o mineral pode ser curvado sem, no entanto, voltar à sua forma original;
- Elástico – o mineral pode ser curvado, voltando à sua forma original quando o forçamento cessa.
Magnetismo
Ocorre nos poucos minerais que devido à sua natureza ferromagnética são atraídos por um íman. Os exemplos mais comuns são a magnetite, a pirrotite e outros com elevado teor de metais que podem ser magnetizados após aquecimento, como o manganês, o níquel e o titânio.
Peso específico (ou densidade relativa)
É a relação do peso de um mineral quando comparado com o peso de igual volume de água. Para isto, o mineral deve ser pesado imerso em água e ao ar. O processo utiliza abalança de Jolly, aplicando a seguinte fórmula:
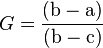
- onde
 é o peso do mineral fora da água;
é o peso do mineral fora da água; 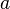 a referência inicial da balança ou calibragem em zero; e
a referência inicial da balança ou calibragem em zero; e  o peso do mineral dentro da água. Assim, por exemplo, se um mineral tem peso específico 3,0 determinada pelo processo descrito, tal significa que ele pesa três vezes mais que igual volume de água.
o peso do mineral dentro da água. Assim, por exemplo, se um mineral tem peso específico 3,0 determinada pelo processo descrito, tal significa que ele pesa três vezes mais que igual volume de água.
Sistema cristalino
A forma do cristal é muito importante na identificação do mineral, pois ela reflecte a organização cristalina da estrutura dos minerais e dá boas indicações sobre o sistema de cristalização do mineral. Algumas vezes o cristal é tão simétrico e perfeito nas suas faces que coloca em dúvida a sua origem natural. Porém, os cristais perfeitos são muito raros, pelo que a maioria dos cristais apenas desenvolve algumas de suas faces.
Classificação química dos minerais
Os minerais podem ser classificados de acordo com sua composição química e são listados abaixo na ordem aproximada de abundância na crusta terrestre.
Silicatos
O grupo dos silicatos é de longe o maior grupo de minerais, sendo compostos principalmente por silício e oxigénio, com a adição de catiões como o magnésio, o ferro e o cálcio. Alguns dos mais importantes silicatos constituintes de rochas comuns são o feldspato, o quartzo, as olivinas, as piroxenas, as granadas e as micas.
Carbonatos
O grupo dos carbonatos é composto de minerais contendo o anião (CO3)2- e inclui a calcite e a aragonita (carbonatos de cálcio), a dolomita (carbonato de magnésio e cálcio) e asiderita (carbonato de ferro). Os carbonatos são geralmente depositados em ambientes marinhos pouco profundos, com águas límpidas e quentes, como por exemplo em mares tropicais e subtropicais. Os carbonatos encontram-se também em rochas formadas por evaporação de águas pouco profundas (os evaporitos, como por exemplo os existentes noGreat Salt Lake, Utah) e em ambientes de karst, isto é regiões onde a dissolução e a precipitação dos carbonatos conduziu à formação de cavernas com estalactites eestalagmites. A classe dos carbonatos inclui ainda os minerais de boratos e nitratos.
Sulfatos
Todos os sulfatos contém o anião sulfato na forma SO4. Os sulfatos formam-se geralmente em ambientes evaporíticos, onde águas de alta salinidade são lentamente evaporadas, permitindo a formação de sulfatos e de halóides na interface entre a água e o sedimento. Também ocorrem em sistemas de veios hidrotermais sob a forma de minerais constituintes da ganga associada a minérios de sulfetos. Os sulfatos mais comuns são a anidrita (sulfato de cálcio), a celestita (sulfato de estrôncio) e o gesso (sulfato hidratado de cálcio). Nesta classe incluem-se também os minerais de cromatos, molibdatos, selenatos, sulfetos, teluratos e tungstatos.
Halóides
O grupo dos halóides é constituído pelos minerais que formam os sais naturais, incluindo a fluorite, a halite (sal comum) e o sal amoníaco (cloreto de amónia). Os halóides, como os sulfatos, são encontrados geralmente em ambientes evaporíticos, tais como lagos do tipo playa e mares fechados (por exemplo nas margens do Mar Morto). Inclui os minerais de fluoretos, cloretos e iodetos.
Óxidos
Os óxidos constituem um dos grupos mais importantes de minerais por formarem minérios dos quais podem ser extraídos metais. Ocorrem geralmente como precipitados em depósitos próximo da superfície, como produtos de oxidação de outros minerais situados na zona de alteração cerca da superfície ou ainda como minerais acessórios das rochas ígneas da crusta e do manto. Os óxidos mais comuns incluem a hematite (óxido de ferro), a espinela (óxido de alumínio e magnésio, um componente comum do manto) e o gelo(de água, ou seja óxido de hidrogénio). São também incluídos nesta classe os minerais de hidróxidos.
Sulfetos
Muitos sulfetos são também economicamente importantes como minérios metálicos, incluindo-se entre os mais comuns a calcopirita (sulfeto de cobre e ferro) e a galena (sulfeto de chumbo). A classe dos sulfetos também inclui os minerais de selenetos, teluretos, arsenietos, antimonetos, os bismutinetos e ainda os sulfossais.
Fosfatos
O grupo dos fosfatos inclui todos os minerais com uma unidade tetraédrica de AO4 onde A pode ser fósforo, antimónio, arsénio ou vanádio. O fosfato mais comum é a apatite, a qual constitui um importante mineralóide, encontrado nos dentes e nos ossos de muitos animais. Esta classe inclui os minerais de fosfatos, vanadatos, arseniatos e antimonatos.
Elementos nativos
O grupo dos elementos nativos inclui os metais e amálgamas intermetálicas (como as de ouro, prata e cobre), semi-metais e não-metais (antimónio, bismuto, grafite e enxofre). Este grupo inclui também ligas naturais, como o electrum (uma liga natural de ouro e prata), fosfinos (hidretos de fósforo), nitritos e carbetos (que geralmente são só encontrados em alguns raros meteoritos).
Minerais dietéticos (ver artigo ‘minerais dietéticos)
Cronologia e Etimologia dos Elementos Químicos


Os elementos químicos serão citados em ordem cronológica, à exceção dos primeiros, conhecidos desde tempos ancestrais e impossíveis de datação.
São dadas para cada elemento, as seguintes informações: nome, símbolo e posição na tabela periódica, data da descoberta ou isolamento, origem do nome, nome do descobridor ou sintetizador e, eventualmente, outras informações relevantes.
Carbono, C, 6 – Conhecido desde tempos ancestrais. Do grego carbo (carvão). Constitui apenas 0,09 % da crosta da Terra mas é o elemento mais importante para a vida. Pode existir como diamante e grafita, em estado livre e combinado. Desde 1985 é conhecido na forma alotrópica molecular C60, o buckminster-fullereno, popularmente “buckyball”, um dos compostos da família dos fullerenos. Seu isótopo 14C, com meia vida de 5730 anos, é importante para a datação arqueológica. O isótopo 13C é importante para a determinação da estrutura de moléculas orgânicas por Ressonância Magnética Nuclear.
Enxofre, S, 16 – Conhecido desde tempos ancestrais. Do sânscrito, sulvere; símbolo do latim, sulphur.
Cobre, Cu, 29 – Conhecido de muitas civilizações antigas, desde 9000 a.C..; do latim Cuprum, de Cyprus, ilha em que foi descoberto e de onde provinha o metal para os romanos. Jóias anteriores a 9000 a.C., confeccionadas com este elemento, foram encontradas no atual Iraque.
Chumbo, Pb, 82 – Metal conhecido desde tempos ancestrais, usado em esculturas egípcias de 5000 a.C. e, pelos romanos, em tubulações de chumbo para distribuição de água; mencionado na Bíblia e no Livro de Job. O símbolo provém do latim plumbum.
Estanho, Sn, 50 – Desde 3500 a.C.. Um dos primeiros elementos metálicos usados pelo homem, no Egito, na liga bronze: 80% Cu, 20% Sn. Nome e símbolo, do latim stannum.O nome inglês, “tin”, reflete a raiz Tinia, deusa etrusca.
Ferro, Fe, 26 – Conhecido desde ca. 1100 a.C.; O uso do ferro deu nome à Idade do Ferro. O símbolo provém do latim, ferrum. Em inglês antigo, “iren”, em alemão, “eisen”.
Prata, Ag, 47 – Conhecida desde tempos ancestrais. Acúmulos de rejeitos de escórias indicam que a prata era separada do chumbo desde 3000 a.C. Do provençal. plata (lâmina de metal); o símbolo Ag deriva do latim argentum.
Mercúrio, Hg, 80 – Conhecido desde tempos ancestrais, por chineses e egípcios; encontrado em tumbas de 1500 a.C. Foi associado ao planeta Mercúrio, deus romano da eloquência, sabedoria e comércio. Em grego, hydrargyrus (hydro = água) + (argyrus = prata), ou seja, prata líquida; o símbolo Hg, do latim hidrargyrum (prata líquida).
Ouro, Au, 79 – Conhecido desde civilizações ancestrais. No sânscrito jval e no anglo-saxônico geolo, significam “ouro”; o símbolo Au, do latim aurum (brilhoso).
Arsênio, As, 33 – Compostos de arsênio eram minerados por chineses, gregos e egípcios, em tempos ancestrais. Em 1250, o primeiro isolamento do metal, pelo alquimista alemão Albertus Magnus. – 1. Do latim arsenicum (masculino, porque antigamente pensava-se que metais teriam sexo); – 2. do grego arsenikon, nome que provém de arsenicum, o ouro-pimento (em inglês, “orpiment”), pigmento amarelo usado nos tempos da Grécia e Roma antigas, por propriedades afrodisíacas.
Antimônio, Sb, 51 – Reconhecido em compostos de civilizações antigas. No Sec. 17, foi identificado como metal. Do grego anti + monos (não sozinho). Símbolo, do latim stibium (marca).
Bismuto, Bi, 83 – Conhecido desde o Sec. 15. – 1. do grego bismuthos (alvaiade de chumbo), porque antigamente era confundido com estanho e chumbo; – 2. do alemão weisse masse (massa branca), depois, wissmuth. Descoberta do elemento, creditada, em 1753, francês Claude Geoffroy, o Jovem.
Fósforo, P, 15 // 1669 – Descoberto pelo médico alemão Hennig Brandt. Do grego phosphoros (portador de luz, porque, por lenta oxidação ao ar à temperatura ordinária brilha no escuro.
Cobalto, Co, 27 // 1735 – Isolado pelo químico sueco Georg Brandt. Há milhares de anos, já era conhecido dos egípcios a fabricação de vidro azul com traços de minerais de cobalto. Kobold, do alemão antigo, gnomo malígno, ou espírito malígno, conhecido dos mineiros e associado ao Nickel, ambos prejudiciais a outros minerais das minas da Alemanha, tornando-os venenosos.
Platina, Pt, 78 // 1741 – Há indícios de uso nas civilizações pré-colombianas nas Américas. Descoberta, em 1741, pelo inglês Charles Wood, que a designou, do espanhol, platina (diminutivo de prata).
Zinco, Zn, 30 // 1746 – Minérios usados em tempos medievais, na China e Índia; no Sec. 13, o primeiro isolamento do metal, na Índia; em 1746, o primeiro isolamento do metal puro, na Europa, pelo químico alemão Andreas Sigismund Marggraf. De zink palavra alemã de origem incerta.
Níquel, Ni, 28 // 1751 – Isolado da nicolita, pelo químico sueco Axel Fredrik Cronstedt. 1. do alemão “Kupfernickel”, que significa cobre falso; 2. do alemão Nickel, nome de um gnomo que, segundo a mitologia, habitava as minas da Alemanha, associada a outro, o Kobalt. (ant. Kobold)
Bismuto, Bi, 83 // 1753 – Identificado por Claude Geoffroy.
Magnésio, Mg, 12 // 1755; 1808 – Reconhecido como elemento, por Joseph Black. Só em 1808, isolado e identificado, por Sir Humphry Davy. Do grego Magnesia, cidade da Tessália, na Grécia antiga.
Hidrogênio, H, 1 // 1766 – Provavelmente descoberto no Sec. 16, por Paracelsus e investigado em 1766 por Henry Cavendish, que mostrou que, da queima do hidrogênio resulta água. Dewar preparou hidrogênio líquido e sólido em 1898. Do grego hydro (água) + genes (formação).
Flúor, F, 9 // 1771; 1886 – Em 1771, primeiramente identificado por Karl W. Scheele. De isolamento dificílimo, devido à extrema reatividade do gás, só 75 anos após, em 1886, foi isolado na forma elementar pura, pelo químico francês F. Henry Moissan, pelo que, recebeu o Prêmio Nobel em 1906. Do latim fluere (fluir), por ser, a fluorita, usada como fluido.
Nitrogênio, N, 7 // Em 1772, primeiramente, produzido pelo químico e físico escocês Daniel Rutherford (“mephitic air”); Priestley (1780) chama-o “phlogisticated air”; Cavendish (1785) produziu ácido nítrico do ar, pelo que, designou-o nitrogen (“niter-producing”). Do latim nitrum e do grego nitron (soda ativa) + genes (formação). Sinônimo obsoleto: azoto. Com 78% do ar, vol/vol, domina a composição da atmosfera terrestre. Composto de nitrogênio de uso mais recente: azida de sódio, NaN3, empregada nos “airbags”, para proteção do motorista de carros; muito explosivo, decompõe-se pelo impacto, liberando grandes volumes de gás.
Cloro, Cl, 17 // 1774 – Descoberto pelo químico sueco Carl Wilhelm Scheele; erroneamente identificado como composto contendo oxigênio. Em 1810, identificado por Sir Humphry Davy como o elemento cloro. Do grego khloros (verde pálido, amarelo esverdeado).
Manganês, Mn, 25 // 1774 – Isolado pelo químico sueco Johan Gottlieb Gahn. Do latim magnesia (íman), pelas propriedades magnéticas da pirolusita, ou lithos magnëtis, pedra magnesiana (de Magnésia, na Tessália). Há também registro da origem de magnesia nigra, não magnética (MnO2), transformada em magnesium, mais tarde em manganese.
Oxigênio, O, 8 // 1774 – O crédito da descoberta é geralmente, dado ao químico inglês Joseph Priestley, mas, Carl W. Scheele, em Uppsala, Suécia, descobriu-o primeiro, só o tendo publicado tardiamente. O crédito pela designação do elemento é de Antoine Laurent Lavoisier, que, incorretamente, pensou que o oxigênio seria necessário à formação de todos os ácidos. Raizes gregas: ox-, oxal-, oxy-, de oxys (ácido) + genes (formação).
Bário, Ba, 56 // 1774; 1808 – Em 1774, o químico sueco Karl Wilhelm Scheele já distinguira a barita da cal. O elemento bário, descoberto e isolado em 1808, pelo químico inglês Sir Humphry Davy. 1. Do grego barys (pesado); 2. de barita, mineral em que foi descoberto.
Molibdênio, Mo, 42 // 1778 – O químico sueco Carl Wilhelm Scheele isolou-o e designou-o, do grego, molybdos (chumbo), por tê-lo isolado da molibdenita (que se pensava ser minério de chumbo; também confundido com grafita (chumbo preto)).
Cromo, Cr, 24 // 1780 – Descoberto por -Nicholas Louis Vauquelin. Do grego khroma (cor) – o metal forma muitos sais coloridos.
Telúrio, Te, 52 // 1782 – Descoberto, na Transilvânia, pelo inspetor de minas e cientista amador alemão Franz J. Müller; só conhecido em 1798, em uma publicação do químico alemão Martin H. Klaproth, que lhe deu o nome, mas registrou o crédito a Müller. Do grego tellus, que significa Terra.
Tungstênio, W, 74 // 1783 – Descoberto por dois irmãos espanhóis – Juan José e Fausto d’Elhuyar y de Suvisa – que o isolaram do mineral volframita, em inglês, wolframite, de onde provém o símbolo. Do sueco tung + sten (pedra dura), por sua alta densidade (19,3 g/cm3).
Zircônio, Zr, 40 // 1787 – O mineral zircônia foi conhecido desde tempos ancestrais. O metal só foi descoberto em 1787, por Martin Heinrich Klaproth. E o metal impuro foi isolado por Jöns Jacob Berzelius, em 1824. 1) de zircão, por ter sido descoberto neste mineral; 2) do persa zargun (cor de ouro).
Estrôncio, Sr, 38 // 1790 – Descoberto e designado pelo cientista irlandês Adair Crawford, que primeiro o identificou na vila escocesa de Strontian, onde foi descoberto. Sais de estrôncio vermelhos são muito usados em fogos de artifício e em tubos de TV a cores.
Ítrio, I, 53 // 1789; 1841 – Identificado, pelo químico finlandês Johann Gadolin. De Ytterby, vila sueca próxima a Estocolmo, de onde proveio o mineral de terras raras.
Urânio, U, 92 // 1789; 1841 – É o último e o mais pesado da série dos elementos naturais. Descoberto em 1789 pelo químico alemão Martin J. Klaproth. Em 1841, o metal foi isolado e identificado pelo químico francês Eugène-Melchoir Peligot. Em 1886, foi identificado pelo físico francês Henri Becquerel como o primeiro dos elementos radioativos; e, em 1944, foi o primeiro elemento usado, por Enrico Fermi, em reação nuclear auto-sustentável, no trabalho de que resultou a bomba atômica. Designado em homenagem ao planeta Uranus, descoberto coincidentemente com o elemento. Sinônimo (obsoleto): uranita.
Titânio, Ti, 22 // 1791 – Descoberto pelo pastor inglês, mineralogista amador, Reverendo William Gregor. Do grego Titans, personagens da mitologia grega (os primeiros filhos da Terra).
Berílio, Be, 4 // 1798; 1828 – Em 1798, foi descoberto pelo químico francês Nicholas Louis Vauquelin, mas só em 1828, foi isolado pela primeira vez, independentemente, por Friedrich Wöhler. Somente em 1957, o metal tornou-se disponível comercialmente. -1. Do grego beryllos (cristal); – 2. De glykis, porque seus sais têm sabor adocicado. 3. Do grego glucinium.
Vanádio, V, 23 // 1801 – Descoberto pelo químico mexicano Andrés Manuel del Rio, que removeu sua reinvidicaçao de crédito, perante a disputa pela descoberta. Redescoberto em 1830 pelo químico sueco Nils G. Sefström. Nomenclatura proveniente de Vanadis, deusa da mitologia escandinava, pela beleza das múltiplas cores de seus compostos.
Nióbio, Nb, 41 // 1801 – Descoberto pelo inglês Charles Hatchett, associado ao tântalo, em uma amostra de columbita. 1. De Niobe, personagem mitológica grega, filha de Tantalo. 2. Nome original, columbio, em homenagem a Cristovão Colombo.
Tântalo, Ta, 73 // 1802 – Descoberto pelo químico sueco Anders Gustav Ekeberg, que o isolou de minerais provenientes da vila sueca Ytterby; mas, o tântalo puro só ficou disponível em 1903. De “Tantalus”, personagem mitológico da Grécia, pai de Niobe, rainha de Tebas, condenado a morrer de sede (alusão ao caráter não absorvente ou à dificuldade em dissolver seus sais minerais em ácido).
Ródio, Rh, 45 // 1803 – Descoberto pelo químico inglês William Hyde Wollaston. Do grego rhodon, por causa da cor rosada de seus sais.
Paládio, Pd, 46 // 1803 – De Pallas, asteróide descoberto em 1802, pouco antes da descoberta do elemento, em 1803, pelo químico inglês William Hyde Wollaston, em uma amostra de platina.
Cério, Ce, 58 // 1803 – Descoberto, simultaneamente, pelo químico sueco Jöns Jacob Berzelius e os químicos alemães Wilhelm Hisinger e Martin Klaproth. Só em 1875 veio a ser preparado na forma metálica pura. De Ceres, asteróide descoberto dois anos antes do elemento.
Ósmio, Os, 76 // 1803 – Descoberto pelo químico inglês Smithson Tennant no resíduo da dissolução de platina em água régia. Do grego osme (cheiro), porque seu tetróxido tem forte odor, prejudicial. Sinônimo: no estado nativo, por vezes denominado osmita.
Irídio, Ir, 77 // 1803 – Descoberto com o ósmio, pelo químico inglês Smithson Tennant, por processo semelhante ao empregado para o ósmio. Do latim iris (arco-iris), pela iridescência de seus compostos, exibindo diversas cores.
Sódio, Na, 11 // 1807 – Isolado e identificado pelo químico inglês, Sir Humphry Davy. Do latim medieval sodanun, medicamento para cefaléia, nos tempos ancestrais; o símbolo provém do latim natrium (carbonato de sódio).
Potássio, K, 19 // 1807 – Isolado por Sir Humphry Davy. Do ingl. potash, pot (pote) + ash, porque, antigamente, queimava-se madeira, ou plantas, em potes (“pot”) de ferro, para produzir a cinza (“ash”), a ser usada como fertilizante. O símbolo provém do latim kalium (álcali).
Boro, B, 5 // 1808 – Isolado pelo químico Sir Humphry Davy e, independentemente, pelos químicos franceses Joseph-Louis Gay-Lussac e Louis Jacques Thénard. 1. do árabe buraq; 2. do persa burah.
Cálcio, Ca, 20 // 1808 – O metal cálcio, foi isolado em 1808 por Sir Humphry Davy. Do latim calx (cal), que já era usada pelos romanos, desde os anos 100 a. C.
Iodo, I, 53 // 1811 – Descoberto pelo químico francês Bernard Courtois. Do grego iödës (cor violeta).
Lítio, Li, 3 // 1817 – Descoberto por Johan August Arfwedson, no laboratório de J. J. Berzelius, em Estocolmo. Do grego. lithos (pedra), porque foi descoberto no mineral rochoso, petalita, contrastando com sódio e potássio, ambos descobertos em cinzas minerais; seu óxido, do grego lithia. Só isolado em 1821, por William T. Brande. Curiosidades: é o elemento metálico mais leve e muito macio, podendo ser cortado a faca; com grande capacidade calorífica, pode absorver grandes quantidades de calor com pequena elevação de temperatura.
Selênio, Se, 34 // 1817 – Descoberto pelo químico sueco Jöns Jakob Berzelius, que o identificou como impureza do ácido sulfúrico de uma fábrica na Suécia. Do grego selene (Lua), por ser semelhante ao do grego Tellus (Terra).
Cádmio, Cd, 48 // 1817 – Descoberto, pelo químico alemão Fredrich Stromeyer. Do grego kadmeia, de “Kadmean earth”, antigo nome da calamina (carbonato de cádmio) e do latim cadmia (carbonato de cádmio), onde foi, primeiramente, descoberto.
Silício, Si, 14 // 1824 – Isolado por Jöns Jakob Berzelius. Do latim silex, silic; silicium (nome dado ao “flint”, silex). É o segundo elemento mais abundante na terra.
Alumínio, Al, 13 // 1825 – Descoberto pelo químico dinamarquês Hans Christian Oersted. Do latim. alumen, alum. Nomes propostos por Davy: alumium ou aluminum; este último, adotado nos Estados Unidos; mas, na Inglaterra e em muitos outros paises, alumínium, com a terminação ium, usual para os metais.
Bromo, Br, 35 // 1826 – Primeiramente, produzido por um estudante de química alemão, mas creditado ao químico francês Antoine-Jérôme Balard, autor da publicação original. Do grego bromos (mau cheiro).
Tório, Th, 90 // 1828 – Descoberto pelo químico sueco Jöns Jakob Berzelius e designado em homenagem a Thor, deus do trovão e ameaças, na mitologia nórdica escandinava. Sua radioatividade passou desapercebida, por ser um processo físico, ainda desconhecido, e, só descoberto em 1897, por Henri Becquerel e o casal Curie.
Lantânio, La, 57 // 1839 – Descoberto pelo químico sueco Carl Gustaf Mosander. Do grego lanthaneis (significa ficar escondido na terra original).
Térbio, Tb, 65 // 1843 – Descoberto por Carl Gustaf Mosander que isolou o óxido a partir do mineral yttria . De Ytterby, vila sueca onde foram encontrados os óxidos naturais de ítrio, Y2O3 e de térbio, Tb2O3
Érbio, Er, 68 // 1843 – Descoberto por Carl Gustaf Mosander que isolou o óxido a partir do mineral yttria. Como no caso do térbio, nome derivado da vila sueca Ytterby, próxima de Estocolmo, onde foi encontrado.
Rutênio, Ru, 44 // 1844 – Descoberto pelo químico russo Karl Karlovich Klaus. De Ruthenia, nome latino da Rússia.
Césio, Cs, 55 // 1860 – Descoberto pelos químicos alemães Robert Bunsen e Gustav Kirchhoff. Do lat. caesius (azul celeste), porque, quando aquecido, emite luz azul; tem duas linhas características na região azul do espectro. Metal curioso: a) baixo ponto de fusão, 29oC, donde, funde na palma da mão; b) Desde 1960, o International Committee of Weights and Measures aprovou o isótopo 133Cs como a medida oficial de tempo, em substituição à fração do tempo de rotação da Terra ao redor do Sol. 1 s = duração de 9.192.631.770 vibrações da radiação emitida pelo 133Cs.
Rubídio, Rb, 37 // 1861 – Descoberto pelos químicos alemães Robert Bunsen e Gustav Kirchhoff, que estudaram o mineral lepidolita. Do latim rubidius (vermelho profundo, cor das linhas espectrais que emite, pelo que, é usado na manufatura de tubos de raios catódicos e de TV).
Tálio, Tl, 81 // 1861 – Descoberto por Sir William Crookes. Do grego thallos (broto verde), pela raia espectral emitida, pela qual foi identificado. Extremamente tóxico: íons Tl3+ são ca. 40×103 vezes mais tóxicos do que o cádmio e afetam diversos orgãos.
Índio, In, 49 // 1863 – Descoberto pelos químicos alemães Ferdinand Reich e Hieronymous T. Richter ao procurar traços de tálio em amostras de minério de zinco. Do latim indicum (índigo, ou violeta), cor da luz brilhante emitida por suas raias espectrais.
Neodímio, Nd, 60 // 1865; 1925 – Lantanídeo, descoberto em 1885, pelo mineralogista amador, Barão Carl Auer von Welsbach, que separou, do mineral didímio, dois sais, um dos quais continha o neodímio, cujo nome vem de neos (novo) + didymos (gêmeo). O outro sal continha o praseodímio. O metal neodímio puro só foi isolado em 1925. No neodímio natural, 24% são do isótopo radioativo 144Nd, com meia vida de 2 milhões de ano.
Hélio, He, 2 // 1868 – Gás nobre descoberto por Pierre Janssen. Do grego Hélios (Sol), por ter sido primeiramente identificado no Sol.
Germânio, Ge, 32 // 1871; 1886 Foi previsto por Mendeleiev, em 1871, em sua tabela periódica, que o chamou “eka-silício”. Em 1886 foi descoberto pelo químico alemão Clemens Winkler, que lhe deu o nome, do latim Germania, nome da Alemanha.
Gálio, Ga, 31 // 1875 – Em 1871, Mendeleiev fez a predição teórica deste elemento, que só veio a ser descoberto espectroscopicamente em 1875, pelo químico francês Paul-Emile Lecoq de Boisbaudran que, no mesmo ano, isolou o metal por eletrólise do hidróxido em KOH. Do latim gallia, nome latino da França, pais do descobridor.
Itérbio, Yb, 70 // 1878 – Primeiro elemento das terras raras descoberto, pelo químico francês Jean de Marignac, no mineral “erbia”, que o designou-o pelo nome da vila sueca Ytterby. Mas o itérbio puro só foi obtido em 1953.
Escândio, Sc, 21 // 1879 – Mendeleiev fez sua predição teórica, mas só em 1879 foi descoberto por Lars Fredrik Nilson, de Uppsala, Suécia, que o designou em honra a seu país natal, Scandia (Escandinávia)
Samário, Sm, 62 // 1879 – Descoberto pelo químico francês Paul-Émile Lecoq de Boisbaudran, que identificara raias do espectro de absorção do elemento no mineral samarskita. O nome é uma homenagem ao oficial do exército russo e engenheiro de destaque, Coronel Samarski.
Hólmio, Ho, 67 // 1879 – Dois cientistas suiços notaram as suas raias espectrais características, mas não conseguiram identificar o elemento, pelo que, chamaram-no elemento X. Logo após, em 1879, o químico sueco Per Teodor Cleve, trabalhando com o mineral “erbia”, isolou e identificou o elemento, nomeando-o por sua cidade natal, Holmia.
Túlio, Tm, 69 // 1879 – O químico sueco Per Teodor Cleve isolou este elemento do seu óxido esverdeado, preparado a partir do mineral “erbia”. O nome provém de Thule, nome ancestral da Escandinávia.
Praseodímio, Pr, 59 e Neodímio, Nd, 60 // 1865 Isolados e identificados por um austríaco
o, mineralogista amador, Barão Carl Auer von Welsbach, que utilizou o mineral chamado didymium, de composição semelhante à da mistura comercial de terras raras da areia monazítica. Depois da eliminação do cério e do tório, ele conseguiu separar dois sais, um contendo o praseodímio e o outro, o neodímio. Só em 1925 o meio neodímio foi isolado. O nome neodímio provém de “neo” (novo) + didymos (gêmeos).
Gadolínio, Gd, 64 // 1886 – Terra rara da série dos lantanídeos. Descoberto pelos químicos franceses Jean de Marignac e Paul-Émile Lecoq de Boisbaudran, que o identificaram a partir da gadolinita. Mineral e elemento designados em homenagem ao químico finlandês Johan Gadolin.
Disprósio, Dy, 66 // 1886 – Terra rara da série dos lantanídeos. Descoberto pelo químico francês Paul Émile Lecoq de Boisbaudron, em uma mistura de óxido de érbio. Do grego dysprositos (dys = mal, difícil) + prositos (encontrar, detectar, isolar). Só em 1950 foi preparado o elemento puro, com o auxílio de técnicas de separação modernas, como a troca iônica
Argônio, Ar, 18 // 1894 – Primeiro gás nobre, descoberto e identificado, por Sir William Ramsay e Lord Rayleigh. Do grego argon (preguiçoso, inativo, qualidade que motivou sua aplicação comercial como enchimento de bulbos de luz incandescente porque evitava a corrosão do filamento de tungstênio). Obtido por destilação fracionada do ar líquido.
Hélio, He, 2 // 1895 – Gás nobre. Em 1868, sua presença no Sol já fora indicada, espectroscopicamente, por Pierre Janssen e Lockyear; descoberto na Terra pelos químicos escoceses Sir William Ramsay e Morris M. Travers, em 1895, proveniente de depósitos terrestres de gás natural. Do grego helios (Sol).
Neônio, Ne, 10 // 1898 – Um dos três gases nobres descobertos ou isolados pelos químicos escoceses Sir William Ramsay e Morris Travers. Obtido por destilação fracionada do ar líquido. Do grego neos (novo). Os átomos dos gases de He e Ar energizados por descarga elétrica, emitem radiação característica, de cor diferente, comumente usada em painéis e em vitrines: a do argônio é púrpura, a do xenônio, azul-esverdeada e a do neônio, laranja avermelhada.
Kriptônio, Kr, 36 // 1898 – Gás nobre descoberto pelos químicos escoceses Sir William Ramsay e Morris M. Travers. Obtido por destilação fracionada do ar líquido. Do grego kryptos (escondido). Desde 1960, o comprimento de onda de uma das cores do espectro de emissão do isótopo 86Kr foi escolhido para definir o metro, que passou a ser exatamente 1.650.762,73 comprimentos de onda da raia espectral vermelho-laranja deste isótopo; e, em 1983, o metro, que era a distância entre duas ranhuras marcadas na barra de platina padrão, armazenada em Paris, foi redefinido, passando a ser a velocidade da luz no vácuo, exatamente 299,792,458 m.s-1. Desde 1963, conhece-se um seu composto fluorado, o KrF4.
Xenônio, Xe, 54 // 1898 – Gás nobre descoberto pelos químicos escoceses Sir William Ramsay e Morris M. Travers. Do grego xenos (estranho). Primeiro gás nobre a ser combinado com platina e flúor, deixando, assim, de ser uma molécula monoatômica para formar um sólido.
Radônio, Rn, 86 // 1898 – Gás nobre descoberto por Friedrich Ernst Dorn. Radioativo de risco.
Polônio, Po, 84 e Rádio, Ra, 88 // 1898 – Descobertos por Marie Slodowska Curie
e Pierre Curie, em 1864. A descoberta do polônio precedeu a do rádio e seu nome foi uma homenagem ao país natal de Marie Curie. Verificando que após a extração do urânio ainda restava radioatividade residual na pechblenda. Eles trataram toneladas do resíduo e nele identificaram, além das raias espectrais do bário, outras, vermelhas, que eles atribuiram ao novo elemento, produto de decaimento do urânio e do tório, o que deram o nome derivado do latim, radius (raio). O elemento só foi isolado quatro anos depois.
Actínio, Ac, 89 // 1899; 1902 – Descoberto duas vezes, independentemente: em 1899, pelo cientista francês André Debierne; e, em 1902, pelo químico alemão Friedrich (Fritz) Otto Giesel. Do grego aktis, aktinos (raio, feixe) porque ele emite partículas ? brilha no escuro. Fortemente radioativo (150 vezes mais do que o rádio), é usado para a produção de neutrons.
Radônio, Rn, 86 // 1900 – Gás nobre descoberto pelo físico alemão Friedrich Ernst Dorn, que lhe deu o nome de emanação do rádio. Outros estudiosos de suas propriedades – William Ramsay e R. W. Whytlaw-Gray mudaram o nome para “niton”, do latim nitens (brilhante), mas desde 1923 é chamado de radônio.
Európio, Eu, 63 // 1901 – Isolado pelo químico francês Eugène-Anatole Demarçay como impureza de uma amostra de samário-gadolínio. O nome é uma homenagem à Europa.
Lutécio, Lu, 71 // 1907 – Descoberto pelo mineralogista austríaco, Barão Carl Auer von Welsbach e pelo cientista francês Georges Urbain. O primeiro quiz denomina-lo cassiopium, pela constelação Cassiopeia, mas Urbain deu-lhe o nome que vingou, baseado no nome antigo de Paris, Lutecia, ou Parisorum, cidade do descobridor.
Protactínio, Pa, 91 // 1913 – Elemento natural, descoberto pelos físicos alemães Kasimir Fajans e O. H. , Göhring, que lhe deram o nome de “brevium”, que, em 1949, passou a protactínio, do grego protos (primeiro) + actinium (nome do nome produto de seu decaimento, o actínio, elemento 89).
Háfnio, Hf, 72 // 1923 – Previsto por Mendeleiev como elemento 72. Foi difícil identifica-lo por causa da interferência do zircônio. Só em 1923 veio a ser descoberto pelos químicos Dirk Coster, holandês, e George Karl von Hevesey, húngaro. Embora nenhum dos descobridores fosse dinamarquês, deram-lhe o nome “Hafnia”, ou “Kjöbnhafn”, nome latino de Copenhagen, em honra a Niels Bohr, porque o elemento foi descoberto através da predição da sua configuração eletrônica, baseada na teoria da mecânica quântica desenvolvida por Bohr.
Rênio, Re, 75 // 1925 – As propriedades do rênio foram previstas, com base na Tabela Periódica de Mendeleiev. Descoberto em minérios de platina pelos químicos alemães Walter Wilhem Noddack, Ida Noddack-Tacke e Otto Carl Berg. Do grego Rhenus (Reno, rio europeu).
Tecnécio, Tc, 43 // 1937 – Descoberto por Carlo Perrier e Emilio Segrè. Identificado no espectro de alguns tipos de estrelas. Foi o primeiro elemento a ser produzido artificialmente. Foi identificado, recentemente, identificado no espectro de diversas estrelas e na Terra. Do grego technetos (artificial) porque sua primeira produção ocorreu em laboratório, a partir de outro elemento.
Frâncio, Fr, 87 // 1939 – Descoberto pela química francesa Marguerite Perey, do Instituto Curie, de Paris, e seu nome é uma homenagem à França, país em que foi descoberto. Muito raro. Existe, na Terra, menos de 30g.
Netuno, Np, 93 // 1940 – Netuno, primeiro elemento transurânico produzido artificialmente por Edwin M. McMillan e Philip H. Abelson, que usaram o acelerador ciclotron da Universidade da Califórnia, em Berkeley, para bombardear o elemento plutônio com partículas alfa. Já foram identificadas quantidades traços de Np naturais, no minério de urânio. Do planeta Netuno, cujo nome provém do deus romano dos mares.
Astatínio, At, 85 // 1940 – Produzido artificialmente, pela primeira vez, pelo grupo de radioquímicos Dale R. Corson, Kenneth R. MacKenzie e Emilio Segrè, na Universidade da Califórnia, Berkeley,que bombardearam um isótopo do bismuto com partículas ?. Do grego astatos (instável). Produto de decaimento do urânio e do tório, é o elemento natural mais raro (a qualquer tempo menos de 30 g).
Plutônio, Pu, 94 // 1941 – Elemento natural que ocorre em quantidades mínimas nos minérios de urânio. Foi o segundo elemento transurânico a ser sintetizado. O químico americano Glenn T. Seaborg e colaboradores usaram o acelerador ciclotron da Universidade da Califórnia, Berkeley. Só em 1946, após o término da II Guerra Mundial, foi divulgada a descoberta deste elemento. No final dos anos de 1960, o Pu foi usado para fornecer energia aos equipamentos eletrônicos na excursão lunar do módulo (LEM) do Apollo. Nome derivado do planeta Plutão.
Amerício, Am, 95 // 1944 – Quarto elemento transurânico descoberto pela equipe de Glenn T. Seaborg, incluindo Ralph E. James, Leon O. Morgan e Albert Ghiorso, que produziram o isótopo 241Am durante a II Guerra Mundial, no Argonne National Laboratories da Universidade. de Chicago. O nome é uma homenagem aos Estados Unidos da América, onde foi descoberto.
Cúrio, Cm, 96 // 1944 – Não ocorre naturalmente. Criado pela equipe de Glenn T. Seaborg, incluindo Ralph A. James e Albert Ghiorso, que usaram o acelerador ciclotron da Universidade da Califórnia, em Berkeley. A identificação quimica foi feita, durante a II Guerra Mundial, no Argonne National Laboratory da Universidade de Chicago. O nome é uma homenagem a Pierre e Marie Curie.
Promécio, Pm, 61 // 1947 – Descoberto por um grupo de cientistas do Oak Ridge National Laboratory (ORNL), L. A. Mirinskiy, I. E. Glendenin e C. D. Coryell, como elemento sintético, ainda não encontrado na crosta da Terra, mas já identificado no espectro de diversas estrelas da galáxia de Andrômeda.Seu nome deriva de Prometeus, deus grego que roubou o fogo do céu. Propriedades químicas ainda pouco conhecidas.
Berkélio, Bk, 97 // 1949 – Não ocorre naturalmente. Produzido pela primeira vez pelo grupo de Stanley Thompson, Albert Ghiorso e Glenn Seaborg, que bombardearam 241Am com partículas ?, no acelerador ciclotron da Universidade. da Califórnia, Berkeley. O nome é uma homenagem à cidade de Berkeley, local de sua descoberta.
Califórnio, 98 // 1950 – Produzido artificialmente pelos cientistas Stanley Thompson, Albert Ghiorso, Glenn T. Seaborg e Kenneth Street Jr., que usaram o acelerador ciclotron da Universidade. da Califórnia, Berkeley, para bombardear 242Cu com partículas ?. O nome é uma homenagem ao Estado da Califórnia, Estados Unidos da América.
Einsteinio, Es, 99 e Férmio, Fm 100 // 1952 – Descoberto por uma equipe de cientistas
liderada por Albert Ghiorso, que investigou fragmentos residuais da explosão do teste da primeira bomba de hidrogênio no Oceano Pacífico. Descobriram, primeiramente, 100.000 átomos de um isótopo do Es e, mais tarde, de Fm. A descoberta só foi divulgada em 1955. Os nomes são homenagens aos físicos Albert Einstein e Enrico Fermi.
Mendelévio, Md, 101 // 1955 – Produzido artificialmente pelo grupo de cientistas liderado por Albert Ghiorso, da Universidade. da Califórna, Berkeley, que usou o acelerador ciclotron para o bombardeamento de einstênio-253 com partículas alfa. O nome é uma homenagem ao químico russo Dmitry Mendeleyev.
Nobélio, No, 102 // 1958 – A descoberta deste elemento foi reinvidicada, em 1957, por um grupo de cientistas do Instituto Nobel, em Estocolmo, que bombardearam um alvo de cúrio com feixe de 13C e observaram partículas ?, que identificaram o elemento 102, nobélio; mas a descoberta não foi confirmada. Em 1958, a equipe de cientistas da Universidade. da Califórnia, Berkeley, liderada por Albert Ghiorso, identificou inequivocamente o isótopo 254No, de vida curta (meia vida 55 segundos). Eles usaram o Acelerador Linear de Ions Pesados (HILAC, acrônimo de Heavy Ion Linear Accelerator) da Universidade de Berkeley, para bombardear uma amostra de 244Cu e 246Cu com 13C. A descoberta foi confirmada por um grupo de físicos russos de Dubna, União Soviética. Ghiorso e colaboradores mantiveram o nome original cunhado pelo grupo de Estocolmo, em honra a Alfred Nobel, descobridor da dinamite.
Laurêncio, Lr, 103 // 1961 – Produzido artificialmente pela equipe de Albert Ghiorso, com Torbjørn Sikkeland, Almond E. Larsh e Robert M. Latimer, que usaram o acelerador HILAC da Universidade. da Califórnia, Berkeley; para produzir o isótopo 258Lr, com meia vida de 4 segundos. Designado em honra a Ernest O Lawrence, ex-Professor da Universidade da Califórnia, inventor do ciclotron.
Ruterfórdio, Rf, 104 // 1964; 1969 – Primeiro elemento dos transactinídeos, criado pela equipe de cientistas liderado por Albert Ghiorso. Descoberta e nomeação disputadas: a descoberta, primeiramente divulgada, em 1964, por um grupo de cientistas russos, do Joint Institute for Nuclear Research (JINR), Dubna, URSS, e o elemento, que, conforme o código de designação da IUPAC, seria designado unnilquadium-260, o “un-nil-quad-ium” (1-0-4-ium), por eles designado, “kurchatovium”, em homenagem ao químico van Kurchatov, chefe de pesquisas soviético. Em 1969, o grupo americano de Ghiorso, usando o acelerador HILAC, de Lawrence Berkeley National Laboratory, da Universidade. da Califórnia, divulgou a identificação positiva do unnilquadium-257, propondo homenagem ao físico neozelandês Ernest Rutherford. Este nome foi confirmado pela American Chemical Society (ACS). Em 1994, em disputa, a IUPAC resolveu dar ao elemento químico 104, o nome “dubnio”, em honra ao centro científico de Dubna. A ACS rejeitou-o. Mas, por decisão final, a descoberta está compartilhada.
Dubnio, Db, 105 (Hânio, Ha, 105) // 1967; 1970 – Descoberta disputadas. Em 1967, o grupo de cientistas russos do JINR., Dubna, URSS, divulgou ter produzido o unnilpentium-260. Em 1970, o grupo da Universidade. da Califórnia, Berkeley, liderado pelo físico norte-americano Albert Ghiorso, usando o acelerador HILAC, identificou inequivocamente o unnilpentium-260, não conseguindo reproduzir os resultados dos colegas russos. Deu ao novo elemento o nome de Hânio em honra a Otto Hahn, descobridor da fissão nuclear. O nome hânio foi endossado oficialmente pela Am. Chem. Soc. Criado pela, IUPAC, em 1985, o Transfermium Working Group, após 5 anos de trabalho, resolveu que o elemento 105 havia sido descoberto independentemente pelos dois laboratórios, e a IUPAC decidiu adotar o nome Dúbnio, para o elemento 105, em reconhecimento ao trabalho do centro de Dubna, URSS.
Seabórgio, Sg, 106 // 1974; 1993 – Transactinídeo cuja descoberta e nomeação foram disputadas. Em junho de 1974, um grupo do JINR, Dubna, URSS, divulgou a produção do elemento 106, unnilhexium; mas a descoberta não foi confirmada. Três meses depois, um grupo de cientistas do Lawrence Livermore Laboratory e da Universidade da Califórnia, Berkeley, liderado por Albert Ghiorso e incluindo Glenn T. Seaborg, divulgou a descoberta inequívoca do uninilhexium-263, usando o acelerador HILAC. Em 1993, o trabalho do grupo de Berkeley foi confirmado, e ele recebeu o crédito da descoberta do elemento 106, que não ocorre naturalmente e do qual só foram sintetizados alguns poucos átomos.Disputa pelo nome: uma comissão internacional da IUPAC tentou impedir o nome “Seaborgium”, porque eo químico nuclear Seaborg, ainda estava vivo. O elemento 106 seria chamado de Ruterfórdio, em homenagem a Ernest Rutherford. A American Chemical Society rejeitou este nome em favor de “Seaborgium”.
Bohrium, Bh, 107 e Hassium, Hs, 108 // 1981 – O grupo do JINR, Dubna, divulgou. em 1976, a síntese do elemento 107, unnilseptium, que não foi confirmada. Em 24 fevereiro de. 1981, os físicos alemães Peter Armbruster e Gottfried Münzenberg, do Laboratório de Pesquisa de Íons Pesados de Darmstadt, Alemanha, divulgaram ter descoberto o elemento artificial unnilseption, e propuseram o nome Nielsbohrium, em honra ao físico holandês Niels Bohr. Em 1992, a IUPAC e a American Chemical Society confirmaram, o nome proposto pelo grupo alemão, como Bohrium.Em 14 mar. 1984, foi identificado, pela primeira vez, o elemento Hassium, Hs, 108, unniloctium, pelo grupo de físicos alemães do GSI, liderados por Armburst e Münzenberg, que propuseram o nome hassium, com base em hassia, nome latino do estado alemão. O Hs transmuta-se em isótopos do Seabórgio, Rutherfórdio, Nobélio e Férmio.As propriedades físicas do Bh e do Hs ainda são desconhecidas.A descoberta foi confirmada pela IUPAC em 1992. Mas, quanto ao nome do elemento 108, a IUPAC iniciou, em março de 1994, uma disputa, propondo “hahnium”, em homenagem ao químico alemão Otto Hahn. A American Chemical Society rejeitou a proposição da IUPAC em favor dos nomes propostos pelos descobridores.
Meitnério, Mt, 109 // 1982 – Produzido artificialmente pelo grupo de cientistas liderado por Peter Armbruster e Gottfried Münzenberg, do GSI, Darmstadt, Alemanha, que, em 1982, divulgaram a descoberta do elemento sintético 109, uninilennium. Eles bombardearam 209Bi com núcleos de 58Fe acelerados. Propuseram o nome Meitnerium, em honra a Lise Meitner, física austríaca que, juntamente com seu sobrinho, Otto R. Frisch, trabalharam com Otto Hahn. Ela foi a primeira pessoa a imaginar a fissão nuclear espontânea como o fracionamento do núcleo do urânio. A reivindicação foi confirmada em 1992 pela IUPAC e pela ACS, e o nome proposto pelos descobridores foi aprovado.
Darmstadcio, Ds, 110 // 1994 – Em novembro de 1994, um grupo de cientistas liderado por Peter Armbruster, do GSI, Darmstadt, Alemanha, divulgou a criação de um novo elemento, de número 110, pelo sistema da IUPAC, ununnilium (1-1-0-ium), já designado Darmstadcio. Em 1995-1996, três diferentes grupos divulgaram a obtenção de quatro diferentes isótopos do elemento 110. O crédito, porém, coube ao grupo internacional de cientistas do GSI. Em 2002, o grupo GSI confirmou seus resultados e a produção de outros isótopos. Os resultados dos grupos do LBNL e de Dubna/LLNL não foram confirmados, e em agosto de 2003, foi confirmada a descoberta como sendo do grupo do GSI, que, a convite da IUPAC, em 16 agosto de 2003, nomearam-no “Darmstadtium”, em homenagem a Darmstadt, Alemanha, onde está localizado o GSI. Está previsto que o elemento 110 seja o superpesado de meia vida mais longa, ca. 100 anos.
Unununium, Uuu, 111 // 1994 – Anunciado em 8 de dezembro 1994, um mês após a criação do elemento 110 pelo grupo internacional de cientistas do GSI, Darmstadt, Alemanha. Ainda é designado como unununium(1-1-1-ium). Estando, na tabela periódica, na coluna do ouro e prata, presume-se que tenha propriedades de metal, com meia vida de cerca de. 10 s.
Ununbiium, Uub, 112 // 1996 – Em 9 de fevereiro de 1996, cerca de um ano após a síntese do elemento 111, o GSI anunciou a criação do elemento 112 pelo grupo liderado pelo físico alemão Peter Armbuster. Segundo o sistema de código da IUPAC, este é o ununbiium, un-un-bi-ium, ou 1-1-2-ium, com meia vida de cerca de 10 s.
Uuq, 114, 116 // Os acréscimos de novos superpesados à tabela periódica dos elementos prosseguem. Segundo divulgações do grupo do JINR/LLNI, o elemento 288114 tem meia vida de cerca de. 3s; e o 292116, meia vida inferior a 50 ?s. Elementos superpesados, além do Lr, não estão confirmados. Há um número de transactinídeos previstos, com meia vida de milhões de anos; a dificuldade reside na síntese.
FONTES:
www.greenpeace.org.br
www.netresiduos.com
www.ecoambiental.com.br
www.inovacaotecnologica.com.br
Dicionário Brasileiro de Ciências Ambientais, 1999
…..
Minérios
Minério

Minério de ferro bandeado
Minerio (do latim minra, mina) é um mineral que é economicamente autossustentável para a sua prospecção e exploração industrial (mineração).
A sua exploração pode ser feita a céu aberto ou ser subterrânea.
O ferro é um metal. Ele costuma ser extraído de um mineral chamado hematita. A hematite é formada principalmente por ferro combinando com o oxigênio. Os minerais dos quais são extraídos metais e outros produtos com vantagem económica são chamados minérios. Desse modo, dizemos que a hematita é um minério de ferro; e o ferro, por sua vez, é um metal. Já a galena é um minério de chumbo, a esfalerita é um minério de zinco, etc.
Os minérios mais comuns ocorrem sob a forma de óxidos, sulfetos, silicatos ou por metais nativos, associados (ou não) a outros minerais como, por exemplo, cobre e ouro.
Os corpos de minério são formados por uma variedade de processos geológicos.
São os minérios que compõem as rochas, por isso os minérios são extraídos das mesmas.
Exemplos de minérios em alguns continentes
- Argentita: Ag2S – para a extração de prata
- Barita: BaSO4 – para a extração de bário
- Bauxita: Al2O3 – para a extração de alumínio
- Berilo: Be3Al2(SiO3)6 – para a extração de berílio
- Blenda: ZnS – para a extração de zinco
- Bornita: Cu5FeS4 – para a extração de cobre
- Calaverita: AuTe2 – para a extração de ouro
- Calcopirita: CuFeS2 – fundamentalmente, para a extração de cobre
- Calcocite: Cu2S – para a extração de cobre
- Cassiterita: SnO2 – para a extração de estanho
- Cinábrio: HgS – para a extração de mercúrio
- Cobaltita: (Co,Fe)AsS – para a extração de cobalto
- Coltan (*) (Columbita – Tantalita): (Fe,Mn)(Nb,Ta)2O6 – para a extração de nióbio e tântalo
- Cromita: (Fe,Mg)Cr2O4 – para a extração de crómio
- Galena: PbS – para a extração de chumbo
- Hematita: Fe2O3 – para a extração de ferro
- Ilmenita: FeTiO3
- Mirabilita: Na2SO4
- Magnetita: Fe3O4 – para a extração de ferro
- Molibdenita: MoS2 – para a extração de molibdénio
- Ouro: Au – associado ao quartzo e à pirite
- Pentlandita:(Fe,Ni)9S8
- Rutilo: TiO2
- Pirolusita:MnO2 – para a extração de manganês
- Scheelita: CaWO4 – para a extração de volfrâmio
- Sperrylite:PtAs2 – para a extração de Platina
- Uraninita ou Pechblenda: UO2 – para a extração de urânio
- Volframite: (Fe,Mn)WO4 – para a extração de volfrâmio
(*) – Coltan é uma abreviatura. É o nome dado à mistura constituída pelos minérios columbita – (Fe,Mn)Nb2O6 – e tantalita – (Fe,Mn)Ta2O6.

